Postura Adattiva – La Percezione del Dolore
24 Settembre 2020
Dolore lombare: evidenze dalla pratica clinica. Studio osservazionale longitudinale su 182 pazienti
2 Novembre 2021SEGNI DI IPOTROFIA
NODULI DI COPEMAN
Potenziali biomarcatori della disfunzione meccanica, Segni di ipotrofia e noduli di Copeman sono presenti in buona parte delle persone con dolori lombari, nella fase clinica vengono spesso trascurati in favore di verosimilmente asintomatiche lesioni discali od ipotetiche alterazioni radicolari.
Essi consistono in uno o più lipomi (a grappolo) che causano dolore alla parte bassa della schiena, spesso evidenziati da alterazioni della funzione meccanica durante stazione eretta, indissolubilmente legati ad alterazioni del trofismo muscolare di gluteo medio, tensore di fascia lata, bandeletta laterale, vasto laterale, peronei ed elevatore lungo delle dita, così rendendo difficili la seduta o qualsivoglia altro movimento. Sembra la loro alterazione sia strettamente legata alla prima fase degenerativa del conflitto in contro-resistenza (CCR).
fig.1
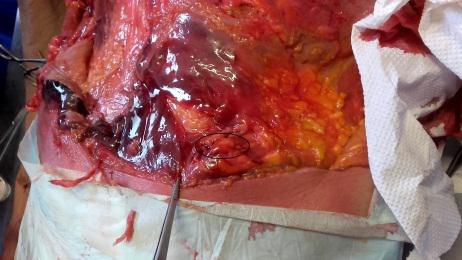
fig.2
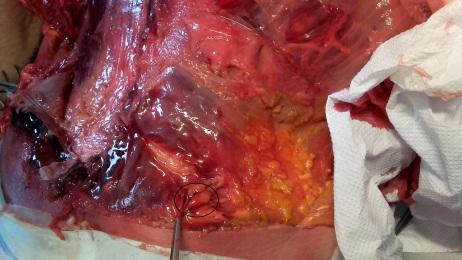
fig.3
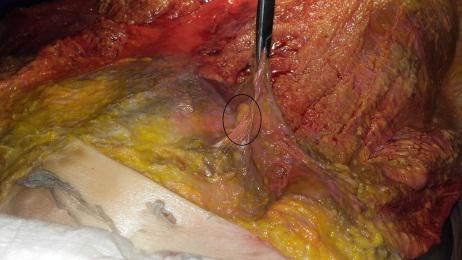
Questa alterazione è stata descritta per la prima volta da Ries nel 1937 come lipoma episacro-iliaco, il cui trattamento include iniezioni di anestetici o escissione chirurgica. Poi da Copeman e Ackerman come “noduli” consistenti in erniazioni del tessuto adiposo attraverso la fascia neurovascolare al di sotto della fascia superficiale (Andreotti, Taddei, pp. 228, 2000), infine da Santoro che, nel periodo 2006-2010, supportato nella clinica dalle evidenze rese da molteplici esami dissettori, identifica questi “noduli” come “lipomi adesi al tessuto fasciale fibroso” ingeneratosi lungo la cresta iliaca (Santoro C., 2012).
All’indagine ecografica appare come una lesione ipoecogena del sottocute, ben circoscritta in corrispondenza della parte superiore della cresta iliaca (in uno o entrambi i lati) non vascolarizzata.
L’esame obiettivo pone in risalto:
-
Fase ispettiva – sensibile riduzione del trofismo (massa muscolare), soprattutto della struttura glutea; postura generalmente antalgica, con la muscolatura lombare paravertebrale in stato di ipotrofismo monolaterale soprattutto nella fase acuta dell’alterazione; rachide lombare tendente a perdere la sua fisiologica lordosi; bacino in disallineamento con contestuale difficoltà alla deambulazione; dolore lombare (segmento di interesse) accentuato dai movimenti del rachide (soprattutto latero-flessione dal lato opposto) e dal ponzare.
fig.4
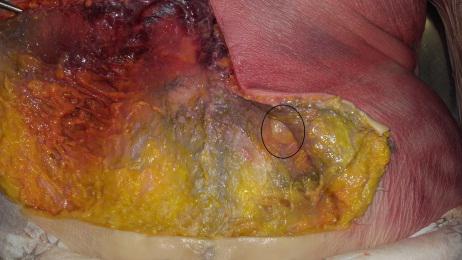
fig.5
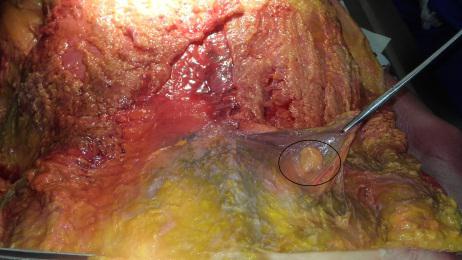
-
Fase palpatoria – strutture nodulari presenti lungo il decorso dell’osso iliaco, la cui palpazione provoca fastidio (iperestesia) o dolore, localizzato o esteso alle gambe (bandeletta laterale, vasto laterale e bicipite femorale, estensore lungo delle dita del piede, peronei, estensore lungo dell’alluce); fibrosità della muscolatura paravertebrale e glutea; deficit della sensibilità (addormentamento) o della funzione muscolare (evidente perdita di forza).
A livello lombo-sacrale, come evidenziato anche attraverso pratica dissettoria condotta presso l’Universitè Bordeaux Segalen (fig. 1-5), questa condizione pone in evidenza due tipologie di segni (ipotrofia tissutale e noduli di Copeman):
-
struttura lipomica (nel numero di una o più per lato), affusolata nella forma e variabile nelle dimensioni (fino a cinque centimetri circa di lunghezza; fino a tre centimetri di larghezza), posta lungo il margine della cresta iliaca, unilateralmente o bilateralmente, incapsulata in tessuto fibrotico rigido, relativamente voluminosa, quando attiva pone il paziente in condizioni da lamentare sintomi riconducibili ad una lombalgia, con dolore urente (trafittivo); quando silente, fastidio.
-
adesione patologica contratta del tessuto fibroconnettivale, avente l’aspetto tipico di una membrana sclerotica ricoprente l’intera fascia toraco-lombare nella sua porzione lombo-sacrale (estensione legata all’intensità e alla durata del processo infiammatorio). Fibrotica e rigida, in sua presenza il paziente lamenta sintomi riconducibili ad una lombalgia, con dolore urente (estensivo).
I tessuti connettivi sono sensibili ad una diminuzione delle forze meccaniche più di quanto non lo siano ad un progressivo aumento (Tipton et al., 1986). Diversi autori (Loitiz et al., 1988; Akenson et al., 1967, 1973, 1986, 1990; Woo et al., 1975, 1982, 1990; Arem e Madden, 1976) hanno rilevato che la mancanza temporanea di stimoli meccanici (periodi di immobilità relativa) genera modifiche strutturali adattive difficilmente regredibili. Cambiamenti che sono riferibili a variazioni nell’orientamento delle fibre del connettivo (Burke e Evans et al. 1960; Enneking e Horowitz 1972; Akenson et al. 1973, 1980, 1986; Videman, 1986; Hardy, 1989; Jaervinen e Letho, 1993), ovvero nella quantità e nella qualità della sostanza amorfa di base (tipica del tessuto connettivo) con una ridotta concentrazione di acqua e glicosaminoglicani (GAGs), da cui una riduzione della lubrificazione interfibrillare e conseguente formazione di aderenze (perdita di capacità di scorrimento) all’interfaccia fibra-fibra (Akeson et al., 1980), otrechè tra tendini e tessuto connettivo circostante. La formazione disordinata di nuove fibre collagene nel tessuto esistente, limita il movimento ed altera la plasticità delle strutture connettivali (Peacock, 1996).
La condizione di immobilità distrettuale cui il corpo viene spesso costretto (lunghi periodi trascorsi in posizione seduta, talvolta in posizione ergonomicamente non idonea) genera dolore e perdita progressiva di funzione, insorta per effetto degli adattamenti connettivali ad una più breve distanza fra l’origine della fibra e la sua inserzione (Viderman, 1986). Il prolungarsi del periodo di immobilizzazione, oltre a generare una repentina degenerazione del tessuto connettivo:
-
dalla terza settimana avvia lo sviluppo di abnormi reticoli tra fibre collagene preesistenti e nuove, alterazione della dinamica del turnover del collagene (sintesi/lisi), deposizione disordinata di nuove fibre collagene all’interno del preesistente tessuto collagene (Loitiz et al., 1988);
-
dalla nona settimana, mostra segni di alterazione della matrice (Akenson et al., 1967, 1973, 1986, 1990; Woo et al., 1975, 1982, 1990; Arem e Madden, 1976).




